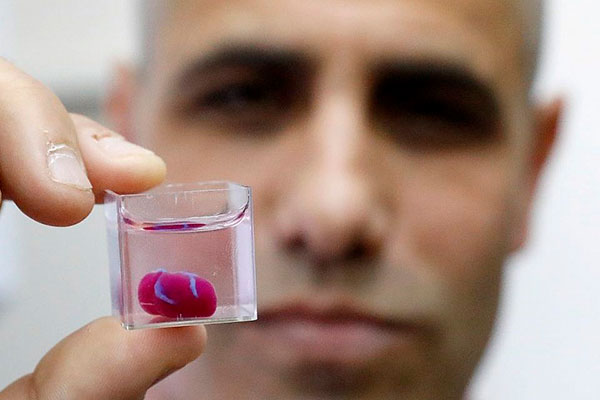
Израиль «печатает» в 3D первую в мире живую злокачественную опухоль головного мозга
Группа израильских исследователей из Тель-Авивского университета распечатала первую в мире жизнеспособную злокачественную опухоль головного мозга с помощью 3D-принтера, воссоздав кровеносные сосуды и окружающую ткань мозга, сообщает «The Jerusalem Post».
«Опухоль глиобластомы основана на образцах, взятых у пациентов во время операции, и окружена сложной системой трубок, похожих на кровеносные сосуды, по которым могут течь клетки крови и лекарства, имитируя реальную опухоль», – пояснила профессор Ронит Сатчи-Файнаро, руководившая исследованием. Глиобластома – самый смертоносный вид рака мозга. Трехмерная модель может помочь ускорить открытие и разработку лекарств или лекарственных препаратов, а также обеспечить новый уровень персонализированной медицины для пациентов, позволяя быстро и надежно прогнозировать наиболее подходящие методы лечения. Исследование было опубликовано 18 августа в рецензируемом журнале «Science Advances».
Работа проводилась совместно с докторантом Леной Нойфельд и финансировалась Фондом Морриса Кана, Европейским исследовательским советом, Израильским фондом исследований рака, Израильской онкологической ассоциацией, Израильским научным фондом и «Check Point Software Technologies».
До сих пор раковые клетки выращивали в двухмерных пластиковых чашках Петри. «Я бы поместила по 1000 клеток в каждую чашку Петри и обработала одну химиотерапевтическим средством», – рассказала Сатчи-Файнаро. «На следующий день или через три дня я ожидаю увидеть уменьшение количества обработанных клеток до 10% от исходных клеток, в то время как контрольные клетки будут продолжать размножаться каждый день».
Когда результаты были хорошими, исследователи рака направляли вещество в клинику. «Мы тестировали новые лекарства подобным образом, по крайней мере, три или четыре десятилетия», – объяснила Сатчи-Файнаро. Но она пояснила, что 90 из 100 соединений, когда они переходят из лаборатории в клинику, не работают. «Это возмутительно! А это значит, что что-то не так. Я начала задаваться этим вопросом. Я дошла до того, что подумала, что, возможно, мы работали с неправильной моделью рака». Что действительно насторожило Сатчи-Фаинаро, так это недавнее исследование, которое она недавно завершила, и в рамках которого ее команда обнаружила белок под названием Р-селектин, вырабатываемый, когда раковые клетки глиобластомы сталкиваются с клетками иммунной системы мозга.
«Мы обнаружили, что этот белок ответственен за сбой в микроглии, заставляя ее поддерживать, а не атаковать смертельные раковые клетки, помогая раку распространяться», – заявила она. «Однако мы идентифицировали белок в опухолях, удаленных во время операции, но не в клетках глиобластомы, выращенных в двухмерных пластиковых чашках Петри в нашей лаборатории». Модель состоит из раковых клеток, а также воссоздает «микросреду мозга» – специализированные глиальные клетки, первичные эффекторные клетки врожденного иммунитета центральной нервной системы и кровеносных сосудов. Сосуды соединены с системой трубок, по которым ученые могут пропускать красные и белые кровяные клетки, и различные лекарства к модели опухоли, чтобы лучше предсказать, что будет эффективно.
«Каждая модель печатается в биореакторе, который мы разработали в лаборатории, с использованием гидрогеля, взятого и воспроизведенного из внеклеточного матрикса, взятого у пациента, тем самым имитируя саму ткань. Физические и механические свойства мозга отличаются от свойств других органов, таких как кожа, грудь или кости. Ткань груди состоит в основном из жира; костная ткань в основном состоит из кальция. Каждая ткань имеет свои свойства, которые влияют на поведение раковых клеток и их реакцию на лекарства», – отметила Сатчи-Файнаро. По ее словам, модель действительно воссоздает важнейшие механические свойства опухоли и среды, в которой она растет, такие, как пластичность и эластичность.
После создания модели команда ученых попыталась доказать, почему она работает лучше, чем пластиковая двухмерная посуда. «Во-первых, мы протестировали вещество, которое подавляет недавно обнаруженный нами белок Р-селектин в культурах клеток глиобластомы, выращенных в двумерных чашках Петри, и не обнаружили разницы в делении и миграции клеток между обработанными клетками и контрольными клетками, которые не получали лечение», – пояснила Сатчи-Файнаро. «Напротив, как в испытаниях на животных, так и в моделях с 3D-биопринтом, которые сверхэкспрессируют белок, мы смогли задержать рост и инвазию глиобластомы, блокируя белок Р-селектин».
Затем ученые провели генетическое секвенирование раковых клеток, выращенных в трехмерной модели, и сравнила их с клетками, выращенными в чашке Петри и в мозгу пациента. Эксперимент показал гораздо большее сходство между опухолями, полученными с помощью 3D-биопечати, и клетками пациента по сравнению с опухолями, выращенными в чашке Петри. «Со временем раковые клетки, выращенные в чашке, утратили всякое сходство с раковыми клетками в образце опухоли головного мозга пациента», – заметила Сатчи-Файнаро. Наконец, они измерили скорость роста опухоли.
«Глиобластома – агрессивное заболевание, отчасти потому, что оно непредсказуемо. Когда гетерогенные раковые клетки вводятся животным, у некоторых рак остается в спящем состоянии, в то время как у других быстро развивается активная опухоль», – подчеркнула она. В чашке все эти опухоли растут с одинаковой скоростью, тогда как в трехмерной опухоли гетерогенность сохраняется. Сатчи-Файнаро рассказала, что ученым потребовалось пять лет, чтобы создать опухоль с 3D-биопечатью.
«У нас было много трудностей и проблем», – подчеркнула она. Но теперь они надеются, что этот прорыв навсегда изменит исследования рака. «Если мы возьмем образец ткани пациента вместе с его внеклеточным матриксом, мы сможем с помощью 3D-биопечати создать из этого образца 100 крошечных опухолей и протестировать множество различных препаратов в различных комбинациях, чтобы найти оптимальное лечение для этой конкретной опухоли», – заявила Сатчи-Файнаро. «В качестве альтернативы мы можем протестировать множество соединений на опухоли с 3D-биопринтом и решить, какое из них наиболее перспективно для дальнейшей разработки и инвестиций в качестве потенциального лекарства. Но, пожалуй, самым захватывающим аспектом является обнаружение в раковых клетках новых подавляемых лекарствами белков и генов – очень трудная задача, когда опухоль находится внутри мозга пациента – человека или животного».
Она отметила, что окончательный план состоит в том, чтобы создать другие модели опухолей, как это было сделано для глиобластомы, например, для опухолей головного мозга, которые развиваются на поздних стадиях рака легких или груди. Они начинают клинические испытания в Медицинском центре «Шиба» в Тель-Хашомере, чтобы проверить этот метод. Если через три – шесть месяцев будет показано, что пациент и модель постоянно реагируют на лечение, «представьте, сколько времени и денег мы сэкономим», – заявила Сатчи-Файнаро. «Наша инновация предоставляет нам беспрецедентный доступ без ограничений по времени к 3D-опухолям, что позволяет проводить оптимальные исследования».